大学院へ行こう!
「大学院に行って、一体何のメリットがあるのか?」そう思ってませんか?
大学院に行くメリット、それは“無から有を創り出す知的体験ができること”あるいは“誰も気がつかなかった事実を発見して、情報を社会に発信する幸福感を手に入れられるチャンスがあること”。
何を大げさなと思うかもしれない。でも、これは本当です。
今、眼科臨床では加齢黄斑変性等の治療に抗VEGF薬の硝子体注射が当たり前のように行われています。眼科医療経済を圧迫していると揶揄されるほどです。しかし、抗VEGF薬が眼科で臨床応用されるようになったのは、ここほんの10年ほどのこと。それまでは影も形もありませんでした。いろいろな原因で虚血状態(循環障害)に陥った網膜が何か液性因子を産生してそれが新生血管を作る。そう考える臨床医が現れなければ生まれなかった治療法です。
前任の根木昭先生はよく「黄斑円孔が治るなんて思いもしなかった」とおっしゃっていました。黄斑円孔とは視力にもっとも影響する網膜の中心に、文字通り穴があいてしまう疾患です。僕が入局した頃、黄斑円孔は不治の病でした。Gassという眼科医が硝子体牽引を解除すれば黄斑円孔を治療できると考えるまでは。その後、黄斑円孔は近代的硝子体手術のもっとも良い適応疾患となりました。
現代は、iPS細胞やIT技術を利用できるのでより多くの発見や発明ができる時代になったはずです。しかし、そうしたテクノロジーの進歩は、一般の眼科医からむしろ研究志向を奪っている側面があるようです。「重要な発見は、こうした最先端の知識と技術をもつ基礎研究者じゃなければ無理じゃないの?」眼科医が研究するなど無意味なのではないか。そう考えてはいないでしょうか。
IOVS(Investigative Ophthalmology and Visual Science)という眼科基礎系トップの雑誌があります。2010年に僕たちのラボからの報告の写真が表紙を飾りました(2010 Sep;51(9):4618-26. doi: 10.1167/iovs.09-4712)。アクアポリンという水チャンネルに関する研究で当時大学院生だった中真衣子先生の仕事です。
水の移動は神経活動に不可欠です。神経細胞に活動電位が生じ、伝播・伝達する際には、細胞内外のイオン環境が激変し、それを是正するために水分子も速やかに移動しなければいけないからです。だから、中枢神経である視神経も水チャンネルであるアクアポリン4を発現しています。しかし、どういうわけか、視神経が眼内に接続している部分、「視神経乳頭」には発現していないことは1998年の段階で知られていました。が、そのまま忘れ去られたのです(図1)。
図1
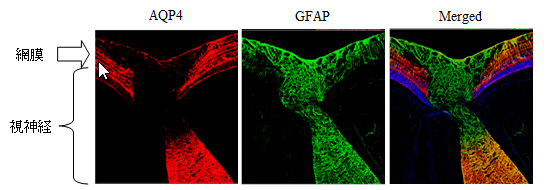
図1.網膜と視神経におけるアクアポリン4の局在。AQP4:アクアポリン4.GFAP:glial fibrillary acidic protein。Merged:重ね合わせ。画像の上方が眼内側、下方が脳側。GFAPはグリア細胞のマーカー。アクアポリン4は網膜内と視神経の脳側にグリア細胞に発現しているが、視神経と網膜の境界部(=視神経乳頭)には発現が見られない。
しかし、この視神経乳頭という場所は、眼科医であればだれでも極めて重要かつユニークな場所であることを知っています。わが国の成人中途失明原因第一位である緑内障。そのターゲットが視神経乳頭だからです。視神経は、視覚情報を伝達する網膜神経節細胞の軸索の集まりです。視神経乳頭に何らかのストレスが加わり、この網膜神経節細胞の軸索が障害されるのが緑内障の初期変化と考えられています。そんな重要で、もっともストレスを受けやすいはずの場所に、神経活動の維持に不可欠と考えられるアクアポリン4が発現していない。これはどうしてだろう?そう思いませんか?
僕達は視神経にはアクアポリンの別のサブタイプ、アクアポリン9が発現していることを見出しました。実は、中枢神経においては、アクアポリン4と9は共発現している箇所が多いのです。視神経もその仲間です。にもかかわらず、視神経乳頭には一つのサブタプしか発現していませんでした。しかも、実験的に緑内障モデルを作成すると、視神経全体からアクアポリン9の発現が消えていきました。すなわち、緑内障では視神経乳頭に一つしか見られないアクアポリン9の発現が抑制されてしまうのです。しかも、アクアポリン9は、水分子だけでなく、エネルギー基質である乳酸等も輸送する特殊なアクアポリン(アクアグリセロポリン)に属しています。このことは、緑内障では視神経乳頭における網膜神経節細胞軸索へのエネルギー供給に障害が起きている可能性を示しています。
本来であれば、一種のニューロサイエンスであるこうした研究は、基礎研究者が真っ先に飛びついてもおかしくないネタに思えます。しかし、僕達が2010年に報告するまで世界中の誰も気がつきませんでした。我々が気づいた理由。それは、「僕達が眼科臨床医だったから」にほかなりません。これこそがまさにclinician scientistの醍醐味です。
アクアポリン9の研究はその後も続いています。昨年には、三木明子先生がAmerican Journal of Pathology誌に論文を掲載しました(2013 May;182(5):1727-39. doi: 10.1016/j.ajpath.2013.01.027)。アクアポリン9は網膜神経節細胞にも発現していて、この発現を強制的に抑制すると、細胞内の活性酸素産生が増え、網膜神経節細胞死が誘導される、という内容です(図2)。
図2
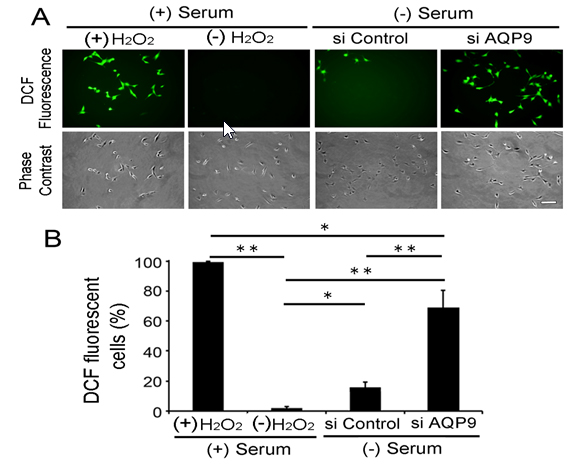
図2.網膜神経節細胞におけるアクアポリン9(AQP9)発現抑制と活性酸素産生増加。
A.活性酸素が生じると緑色の蛍光を発するDFC染色(上段)と位相差顕微鏡像(下段)。Serum:培養液中の血清。H2O2:過酸化水素。Si Control:コントロール配列の導入。Si AQP9:アクアポリン9を抑制する配列の導入。
B.定量グラフ。過酸化水素をかけると((+)H2O2)、ほぼ全ての細胞がDFC蛍光をもつ(つまり活性酸素を産生する)のに対して、血清が存在し((+)Serum)、過酸化水素をかけなければ、ほとんどの細胞は活性酸素を産生しない。血清を除くと((―)Serum)、対照(si Control)でも20%ほどは活性酸素を産生するが、アクアポリン9を抑制すると(si AQP9)70%程度の活性酸素産生細胞の割合が増加する。(Miki A, et al. Loss of aquaporin 9 expression adversely affects the survival of retinal ganglion cells. Am J Pathol 2013: 182(5): 1727-1739. Figure 5を出版社の許可を得て転載)
この雑誌は基礎系の教室でもacceptされるのは簡単ではありません。僕たちの仕事が非常にimpactのあるものだと世界が認識してくれたものと思い、アクアポリン9の網膜神経節細胞の生存に及ぼす影響を今さらに追跡しています。こうした研究を重ねることは、緑内障を始め、未だ根本的治療法が確立されていない疾患の病態の解明につながることでしょう。
目の前の患者を治療する喜び。それは臨床医に与えられた特権です。一方で、今治すことの難しい患者から未来の治療法を確立する突破口を見出す努力。これは臨床医が課せられた使命です。しかもその使命は、若いあなたが、人生の一時期、あるいは一生を捧げても燃やすに足る、高邁で、知的好奇心にも満ちたresearch mindに他ならないのです。神戸大学眼科はアクアポリン9研究以外にも多くのprojectを走らせています。あなたもその仲間になりませんか?
……青春は何もかも実験である
(ロバート・ルイス・ステイーブンソン)
(なお、専門医受験資格との兼ね合い、理研などへの国内留学、clinical courseの詳細等、不明な点や聞きたい点があれば、いつでもmanakamu@med.kobe-u.ac.jpまでメール下さい。)


